2021. 5. 7. 04:04ㆍ배움터: 입시와 공부법
화학에서 기본적으로 배우는 주기율표는
원자 각각의 존재를 알고 외우기 위해서 보통 공부한다.
이런 원자들의 특성이 조금이나마 쓰이는 부분이 있는데
이런 자연 원소들의 전기적 특성들을 파악하고
실생활에서 어떻게 적용되는지를 알아보기 위함이라고 할 수 있다.
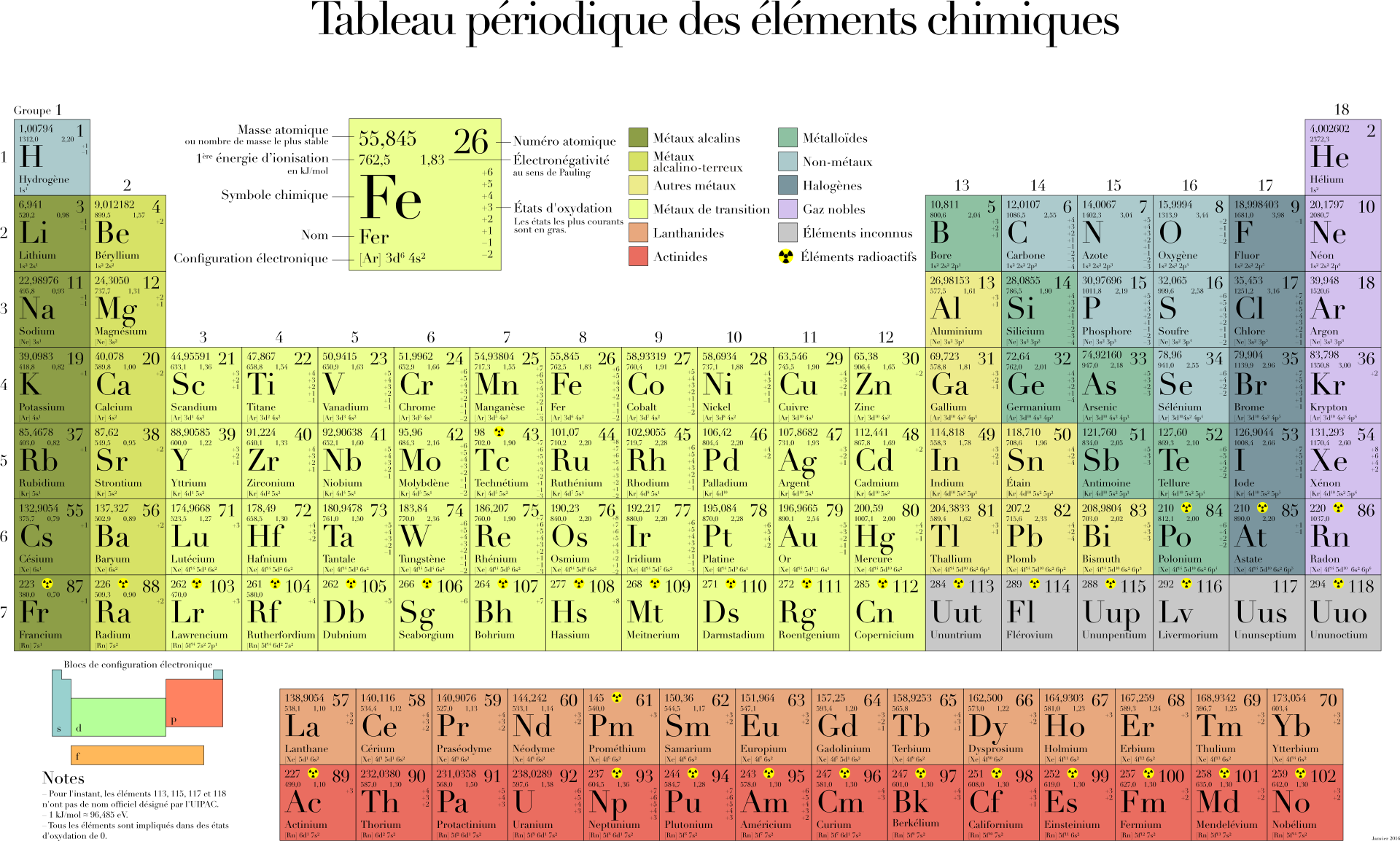
주기율표의 첫번째 원자인 H(수소)의 빛 스펙트럼은
햇빛의 연속 스펙트럼이랑 비교했을 때
스펙트럼 선이 불연속적이고 선마다 색이 다르다.
헬륨, 네온 등 다른 원자의 스펙트럼도 이와 같이 각각 다른 스펙트럼 선의 위치와 색을 나타낸다.
태양광의 흡수 스펙트럼을 조사했을 때 수소 스펙트럼 선이 보이는 조사 결과를 보면
태양 근처에 수소가 있다는 것을 알 수 있다는 증거가 된다.
이렇게 관측 도구를 가지고 물질의 다른 특성을 알 수 있는 건
원자들이 각자가 모두 전기적 특성을 가지고 있다는 공통점 때문이다.
원자는 알다시피 원자핵과 전자로 이루어져 있고
이 구조는 지금에서야

이런 식의 형태로 원자가 생겼다고 배우고 있지만
이전부터 원자가 어떻게 생겼냐는 진화적으로 계속 바뀌어 왔다.
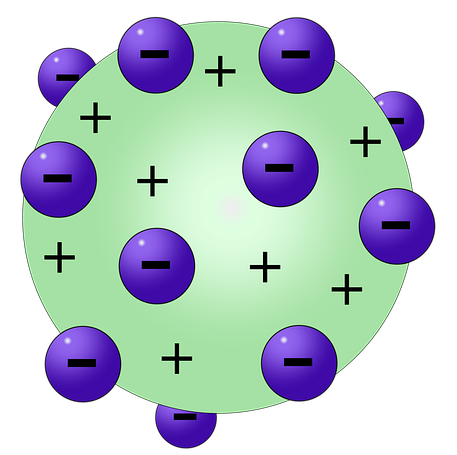
이렇게 양전차와 전자가 여기저기 구슬처럼 붙어있는 형태로 처음에는 가정을 했었다.
그 다음에 나온게
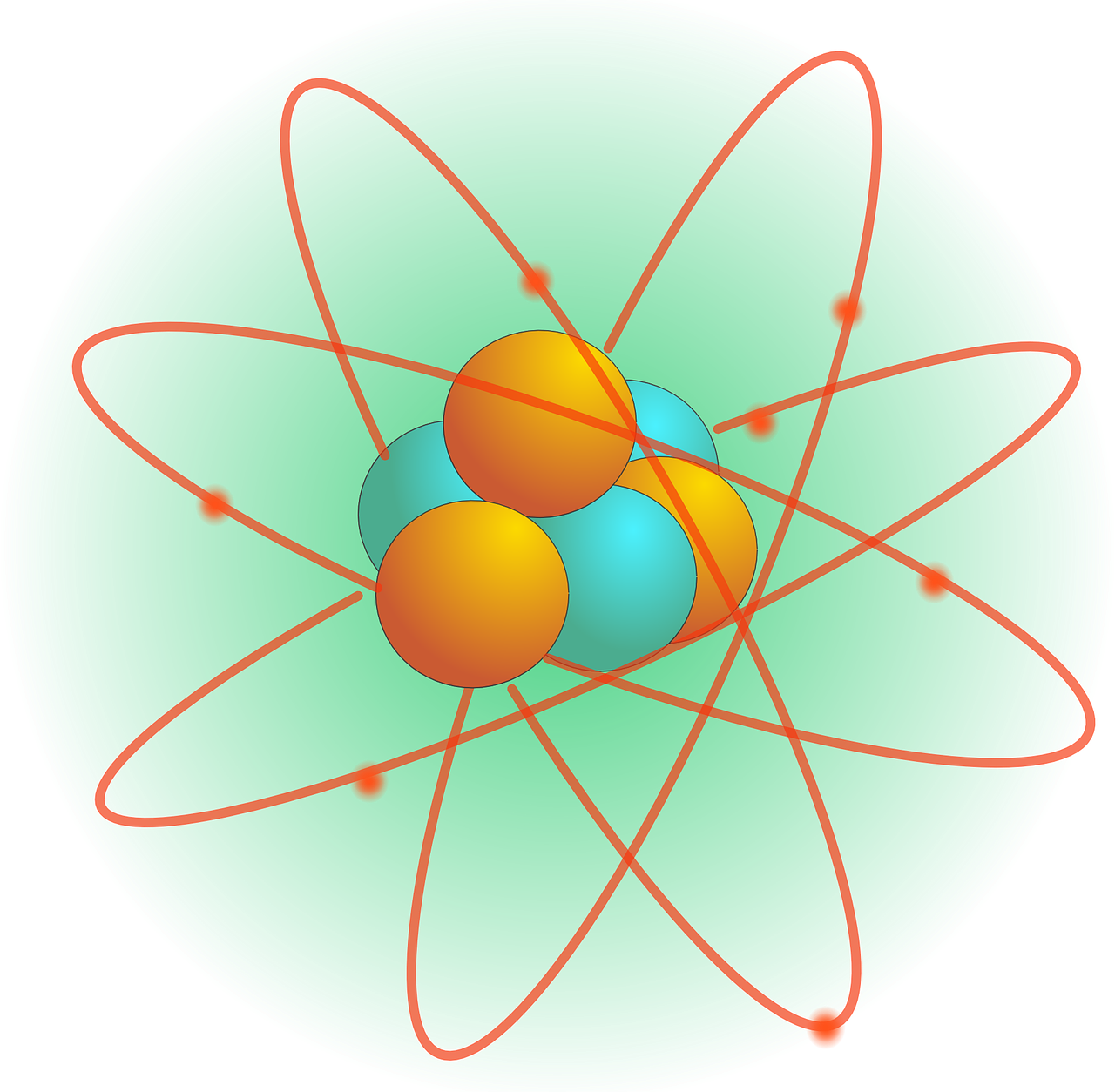
원자핵을 중심으로 전자들이 임의의 원궤도를 중심으로 돌고 있는 형태이다.
그다음에 와서야 지금처럼 태양계의 모습처럼 원자핵을 중심으로 n=1,n=2,n=3 등으로 원형의 나열 형식으로 되어있다고 배우고 있다.
여기서 n=1의 원은 원자핵과 가장 가까이 있고 에너지의 값이 가장 낮다.(준위가 낮음)
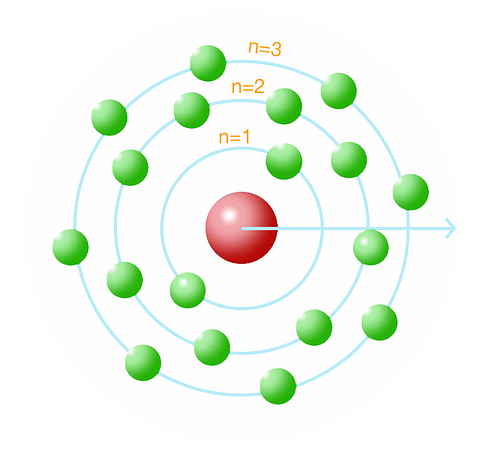
그래서 이 원자가 빛 에너지를 흡수했을 때는 전자가 n=2 쪽으로 그 다음엔 n=3 쪽으로 이동하게 된다.
반대로 빛 에너지를 방출했을 때는 전자가 n=3에서 n=1쪽으로 오게 된다.
빛
E=hf(h=플랑크 상수, f=주파수(진동수)
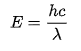
로도 나타낼 수 있는데
f가 c/ㅅ
즉 진공에서의 빛의 속력/파장이 주파수 혹은 빛의 진동수가 됨을 의미한다.
그래서 파장이 짧은 빛(보라색)일수록 진동수가 많아지고
파장이 긴 빛(빨간색)일수록 진동수가 적어짐을 알 수 있다.
여기서 파장이 짧을 수록 빛의 에너지 값도 커짐을 알 수 있다.
그래서 가스레인지 불을 켰을 때 나오는 파란 불과 주황불을 보았을 때
파란색의 불이 스펙트럼 상에서의 에너지 준위가 크다고 말할 수 있고 빛의 에너지가 크고 주파수 또한 높다고 할 수 있다.(파장이 주황색 불보다 짧거나 속도가 빠르거나 라고 표현도 가능)
또한 이렇게 파장이 짧거나 길어도 우리 눈에 안보이는 빛이 있는데
감마선, x선, 자외선이라고 할 수 있다.
이들은 파장이 너무 짧고 주파수도 높아서 우리 눈에 보이지 않는 '비가시광선' 이라해도 문제가 없다.
반대로 적외선은 한의원에도 가면 보이는 붉은 빛 같은 걸로 가시광선(빨강~보라)보다 파장이 길고 주파수가 낮아 우리눈에 잘 보인다.
라이먼 계열
발머 계열
파셴 계열은
스펙트럼으로 나타내는 수소를 보여주는 선의 종류이다.
아래 그림을 보면
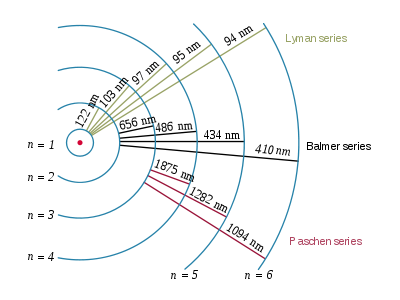
n이 먼 곳에서 n=1로 가는 에너지 방출 상태.
그래서 전자가 n=1로 가는 상태를 라이먼 계열의 선 스펙트럼이다.
아래와 같이 선 간의 간격이 아주 좁은 걸 알 수이따..
결국 에너지가 방출될 때의 에너지의 크기가 엄청 크고 파장이 짧은 걸 보여준다.
그 다음 n=2로의 이동을 발머 계열
n=3로의 이동을 파셴 계열이라고 부른다.
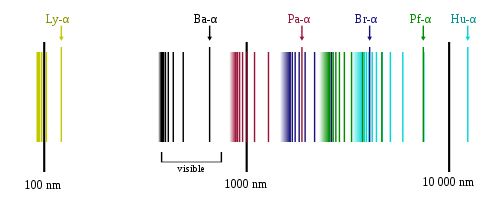
차례대로 보면 에너지 방출량이 갈수록 적어지기 때문에
스펙트럼 선 간의 간격도 넓어지고 파장도 길어지는 걸 알 수 있다.
(아래 그림 중 Br, Pf, Hu는 생략)
'배움터: 입시와 공부법' 카테고리의 다른 글
| 넷플릭스 한영 동시자막으로 영어 공부하는 법 (6) | 2023.10.24 |
|---|---|
| 오늘의 트렌디 영어사전(21.11.17) (0) | 2021.11.17 |
| 2022 문학-현대소설 이광수,무정&김유정,떡) (0) | 2021.04.12 |
| 2022 물리학1-힘과 뉴턴 운동 법칙) (0) | 2021.04.11 |
| 2022 문학 중 시적 표현과 형식-신석정,들길에 서서 (0) | 2021.04.11 |
